解读从干细胞到神经元的旅程研究揭示转变背后持续的基因表达变化
发布时间:2024-07-26 11:46:46 编辑:熊雁星 来源:
日本理化学研究所(RIKEN)的研究人员发现了基因表达模式的逐渐变化如何推动小鼠神经干细胞(NSC)的细胞命运转变。
中枢神经系统中所有主要的神经元类型的细胞都是通过NSC分裂成中间祖细胞(IPC)而产生的,而中间祖细胞又分裂成成熟的神经元。
从NSC到IPC的转变被认为是一个离散事件,因为IPC缺乏与NSC相同的多能性和放射状形状,并且没有细胞表现出NSC和IPC之间的中间特征。然而,单细胞RNA测序分析表明,基因表达从NSC到IPC不断发生变化。
因此,虽然转变看起来很突然,但基因表达的潜在变化是在分化过程中逐渐进行的。
日本理化学研究所脑科学中心主任RyoichiroKageyama对这种明显相互矛盾的证据很感兴趣。“我们想调和这些相互矛盾的观察结果,”他说。
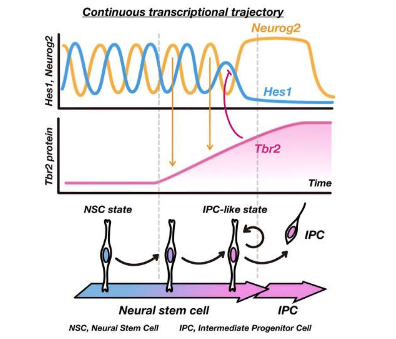
转录因子是控制基因表达的蛋白质。此前,Kageyama团队已证明,调节NSC分化的转录因子以振荡方式表达。特别是,转录因子Hes1的表达振荡抑制促进神经元细胞命运的基因(如Neurog2)的表达,使NSC在NSC状态和IPC样状态之间交替。
“具有IPC样状态的NSC在细胞分裂后会分化为IPC,”Kageyama指出。
现在,Kageyama和两位同事揭示了在小鼠大脑皮层发育过程中抑制Hes1表达从而诱导小鼠NSC中IPC样状态的机制。
三人发现,Hes1调控的Neurog2振荡会导致T-box脑蛋白2(Tbr2)的积累,T-box脑蛋白2(Tbr2)是一种转录因子,可与Hes1启动子结合以关闭Hes1表达。这项研究发表在《发育细胞》杂志上。
“当Tbr2达到一定水平时,它会有效抑制Hes1,从而推动IPC分化,”Kageyama说。
暂时消除Tbr2表达导致Hes1表达增加并降低NSC分化,证实Tbr2在驱动NSC逐渐转化为IPC中起关键作用。
发现NSC表现出分化细胞样基因表达模式以及干细胞中典型的基因表达模式令人吃惊。“NSC的基因表达模式比以前想象的更加多样化,”Kageyama说。
由于目前的数据表明,振荡基因表达状态对于NSC的多能性和有效增殖非常重要,Kageyama团队打算探索这些振荡基因表达状态如何促进NSC中的细胞周期进程。
